Home » Methodology
Category Archives: Methodology
Enantioselective Total Syntheses of Pallambins A-D
DOI: 10.1002/anie.201907523 full text link
文献汇报人:张昕平
汇报日期: 2019年10月26日
图文摘要:

- 推荐原因:
贾彦兴课题组在不使用保护基的情况下,从已知的环己烯酮8出发,用15-16步反应完成了pallambins A-D的首次不对称全合成。他们通过Pd-催化氧化环化构建[3.2.1]-双环结构,Claisen重排/内酯形成序列构建C环,分子内Wittig反应形成D环。在此过程中,作者还开发了一种温和的a-溴代酮脱溴化氢方法。
Asymmetric Total Synthesis of Cyclocitrinol
J. Am. Chem. Soc. 2018, 140, 5365−5369 DOI: 10.1021/jacs.8b02629 full text link
文献汇报人:张昕平
汇报日期: 2019年6月22日
图文摘要:

- 推荐原因:李闯创教授通过自己课题组发展的type II型分子内环加成反应构建了双环[4.4.1]桥环骨架,并基于此完成了天然产物Cyclocitrinol 的首次不对称全合成。整个合成过程简洁高效。
The Diels-Alder Reaction:Selected Practical Methods
The Diels-Alder Reaction: Selected Practical Methods, Francesco Fringuelli and Aldo Taticchi full text link
文献汇报人:章青余
汇报日期: 2019年03月30日
图文摘要:

- 推荐原因:
Diles-Alder Reaction是一类非常有名的有机环加成反应,它能通过区域及立体控制的方法广泛用于构建六环体系,并且得到最多四个立体中心。因为Diles-Alder Reaction能高效地构建复杂的的体系,越来越多的合成策略都选择去应用它,因此非常有必要去了解这个反应。这本书以实际例子从各个方面非常详细地描述Diles-Alder Reaction,值得我们学习。
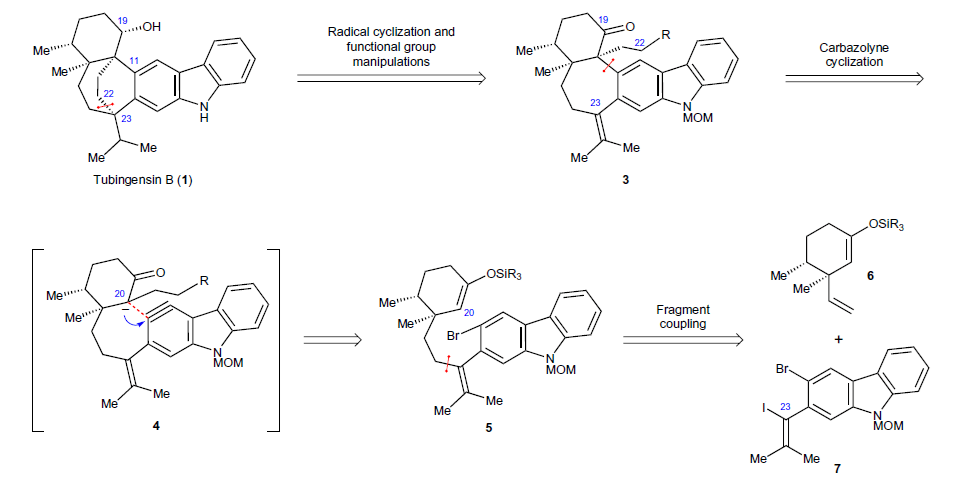
Total synthesis of (–)-tubingensin B enabled by the strategic use of an aryne cyclization
Nat. Chem. 2017, 9, 944, DOI: 10.1038/nchem.2801 full text link
文献汇报人:张昕平
汇报日期: 2019年1月19日
图文摘要:
- 推荐原因:
Tubingensin B的结构看似简单,但两个相邻的C(sp2)-C(sp3)键以及与咔唑相连的两个季碳手性中心都是合成的难点,更为挑战的是与咔唑稠合的双环-[3.2.2]-壬烷和高度官能化的六元环部分。该天然产物共含有5个手性中心,其中3个是季碳中心,而且有2个季碳中心还相邻。作者通过芳炔环化策略作为关键步对Tubingensin B进行了高效的全合成。这种利用芳炔环化策略构建多种复杂结构(例如构建相邻的季碳手性中心)的思路,值得深入学习研究。
Cascade Claisen Rearrangement:Rapid Synthesis of Polysubstituted Salicylaldehydes and Total Syntheses of Hemigossypol and Gossypol
Self-Assembled “the intramolecular enolate oxidative couplingreaction
J. AM. CHEM. SOC. 2010, DOI: 10.1021/ja106739g
full text link
文献汇报人:张振
汇报日期: 2018年9月30日
图文摘要:

- 推荐原因:
烯醇负离子氧化偶联反应早在1935 年就已经有报道,各种含羰基的官能团如酸、酯、酮、酰胺甚至吲哚等都能参与该反应。由于分子间反应趋于发生自身二聚及多聚反应,但分子内反应可以很好地控制化学选择性,获得较好的收率。该类方法能够高效地构建1,4-二羰基官能团,在合成上有着较广的应用。
Quick Access to the Framework of Aspidosperma alkaloids skeleton
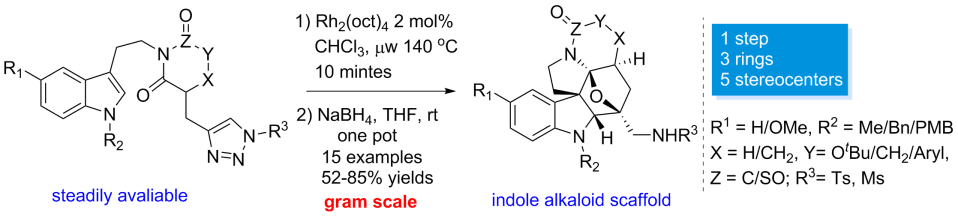
A Rh(II)-catalyzed dearomative intramolecular [3 + 2] dipolar cycloaddition involving the indolic C2−C3 carbon−carbon double bond has been developed. The reaction was launched from the triazole moiety within the substrate and proceeded efficiently under mild conditions. A wide range of functional groups could be tolerated. These features render the
current reaction a highly useful tool for the synthesis of polycyclic indole alkaloids, as showcased by a rapid assembly of the core structure of Aspidosperma and the related alkaloids.